Євросоюз вважає, що Британія дуже швидко схвалила вакцину проти Covid-19
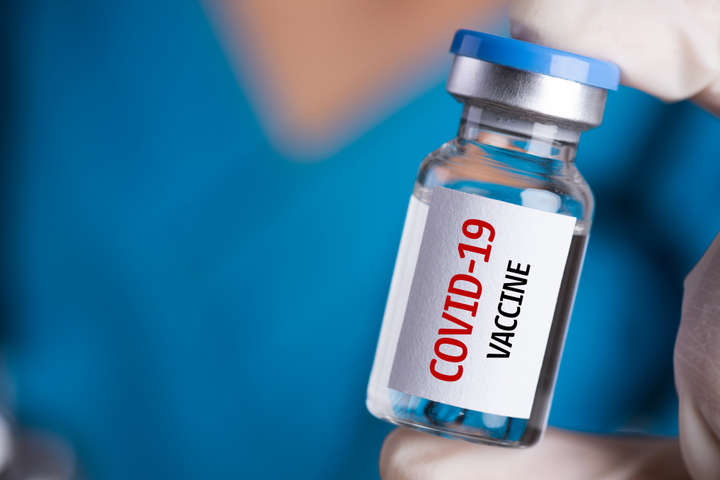
Німеччина заявила, що швидке затвердження вакцини може викликати недовіру до неї у людей
Європейське агентство з лікарських засобів (ЕМА) розкритикувало швидке затвердження Великою Британією вакцини проти Covid-19 заявивши, що його власна процедура є більш ретельною. Про це повідомляє The Guardian.
Зазначається, що управління з регулювання лікарських засобів і товарів медичного призначення Великої Британії (MHRA) затвердило вакцину Pfizer/BioNTech для екстреного застосування всього через 10 днів після того, як почало вивчати дані широкомасштабних випробувань препарату.
Агентство EMA, яке відповідає за затвердження вакцин проти Covid-19 для ЄС, виступило із заявою, щоб підтвердити свій власний «надійний» підхід.
Агентство заявило, що держави-члени ЄС також можуть обрати шлях екстреного затвердження вакцин, однак його власний процес схвалення є «належним регулюючим механізмом у поточній надзвичайній ситуації пандемії, щоб надати всім громадянам ЄС доступ до вакцини та підтримати масову кампанію з вакцинації».
Агентство відзначило, що його процедура вимагає більше перевірок, ніж екстрена процедура, обрана Британією.
У вівторок агентство заявило, що до 29 грудня вирішить, чи затвердити використання вакцини Pfizer/BioNTech у ЄС.
Представник Європейської комісії у середу заявив, що процедура EMA є «найефективнішим регуляторним механізмом», оскільки вона базується на більшій кількості доказів.
Міністр охорони здоров'я Німеччини Єнс Спан сказав, що Берлін також розглядав прискорену видачу дозволу, яку обрала Британія та яка є дозволеною законодавством ЄС. Але, за його словами, переконати людей в безпечності вакцини має вирішальне значення.
«Ідея полягає не в тому, що ми перші, а в тому, щоб мати безпечні та ефективні вакцини в умовах пандемії, і що ми можемо створити довіру, немає нічого важливішого, ніж довіра щодо вакцин», ─ сказав він.
9 листопада компанії Pfizer та BioNTech оголосили про те, що їхня вакцина продемонструвала ефективність у понад 90% на фінальному етапі випробувань. Суттєвим мінусом вакцини є умови її зберігання, адже необхідні спеціальні холодильні установки з температурою понад 70 градусів за Цельсієм.
16 листопада американська компанія Moderna заявила, що ефективність її вакцини-кандидата від Covid-19 становить 94,5%. Очікується, що вакцина Moderna не буде доступна за межами США до наступного року.
Нагадаємо, США отримали першу масову поставку Covid-вакцини.
До слова, ще одна вакцина від коронавірусу проходить затвердження у ЄС.
Крім того, Україна отримає $100 мільйонів на вакцину від Covid-19.
Дата початку поставок в Україну вакцин проти коронавірусу в рамках міжнародної ініціативи Covax стане відома після 7 грудня 2020 року.
Стало відомо, хто в Україні отримає перші вакцини від коронавірусу.
Також очільник МОЗ Максим Степанов розповів про випробування української вакцини від Covid-19.


Коментарі — 0